- Fosfodiester: Es un tipo de enlace covalente que se produce entre un grupo de hidroxilo en el carbono 3.
- Enlaces N-glicosídicos: Es el enlace mediante el cual se unen entre si dos o mas monosacaridos.
- Ester fosfórico: Es un enlace que al romperse libera gran cantidad de energía (contenido en el ATP)
- Hemiacetálico: Es una molécula que contiene un grupo hidroxilo OH y un residuo alcoholxido unido a un átomo de carbono.
2. La cromatina resuelve el problema de restricción de crecimiento de ADN y núcleo, la cromatina está formada por ADN y proteínas, la principal proteína formadora son las histonas.
-Verdadero, ya que se constituye por ellas.
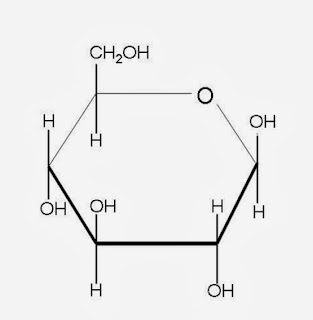
3. Aldopentosa: Monosacárido de cinco átomos de carbono con un grupo funcional aldehído.
4. Saponificación: El método de saponificación en el aspecto industrial, es el que consiste en hervir la grasa en grandes calderas, añadiendo lentamente sosa cáustica (NaOH), agitándose continuamente la mezcla hasta que comienza ésta a ponerse pastosa.
-Verdadero, ya que si cumple con que el ácido graso y el alcohol están unidos
5. Molécula anfipática: hace referencia a una estructura molecular que contiene dos propiedades, una hidrofílica (afinidad por el agua) y otra hidrofóbica (rechazo del agua). Estas moléculas son los principales constituyentes de la membrana celular, generando un sistema al que se le denomina mosaico fluido.
-Verdadero, ya que en las dos partes que se divide si son la hidrofílica y la hidrofóbica.
6. Los 20 aminoácidos que forman parte de las proteínas son: Serina (Ser,S), Treonina (Thr,T), Cisteína (Cys,C), Asparagina (Asn,N), Glutamina (Gln,Q) y Tirosina (Tyr,Y), Glicina (Gly,G), Alanina (Ala,A), Valina (Val,V), Leucina (Leu,L), Isoleucina (Ile,I), Metionina (Met,M), Prolina (Pro,P), Fenilalanina (Phe,F) y Triptófano (Trp,W), Ácido aspártico (Asp,D) y Ácido glutámico (Glu,E), Lisina (Lys,K), Arginina (Arg,R) e Histidina (His,H)
-No todos los aminoácidos son proteínas aunque su mayoría si.
7. Vitamina A: Los diferentes carotenos se transforman en vitamina A en el cuerpo humano. Se almacena en el hígado en grandes cantidades y también en el tejido graso de la piel (palmas de las manos y pies principalmente), por lo que podemos subsistir largos períodos sin su aporte. Se destruye muy fácilmente con la luz, con la temperatura elevada y con los utensilios de cocina de hierro o cobre.
La función principal de la vitamina A es la protección de la piel y su intervención en el proceso de visión de la retina. También participa en la elaboración de enzimas en el hígado y de hormonas sexuales y suprarrenales. El déficit de vitamina A produce ceguera nocturna, sequedad en los ojos (membrana conjuntiva) y en la piel y afecciones diversas de las mucosas. -Verdadero, la vitamina A se sintetiza a partir de carotenoides.
8. Transporte del colesterol: La mayor parte del colesterol se transporta en la sangre unido a proteínas, formando unas partículas conocidas como lipoproteínas de baja densidad o LDL.
-D, se transporta unido a las proteínas formando lipoproteinas.
9. Molécula de agua: Está compuesta por dos átomos de hidrógeno y uno de oxígeno unidos por un enlace covalente. Es decir, los dos átomos de hidrógeno y el de oxígeno se unen compartiendo electrones. Su fórmula es H2O.
-Falso, son dos de hidrógeno y una de oxigeno.
10. La doble hélice del ADN: Se forma ( y estabiliza) mediante puentes de hidrógeno entre las bases nitrogenadas de una hélice y las de otra según el principio decomplementariedad: la Adenina siempre se une a la Timina y la Guanina a la Citosina (de modo que sabiendo la secuencia de una cadena se deduce rápidamente la otra).
-Verdadero, las dos cadenas que conforman al ADN estan unidas por enlaces covalentes.
11. Cerebrósido: Todo lípido formado por galactosa, esfingosina y un ácido graso. Los cerebrósidos son abundantes en las membranas de las células del sistema nervioso y especialmente en las vainas de mielina.
-Falso, son glucolipidos en los que las ceramidas se unen formando un monosacarido
12. Polisacáridos: Son biomoleculas formadas por la unión de una gran cantidad de monosacaridos que se encuentran entre los glucidos y cumplen funciones diversas sobre todo de reservas energéticas y estructurales. Llevando a que los polisacáridos conserven las mismas propiedades físicas que los monosacaridos.
-A, conserva las mismas propiedades físicas que los monosacaridos.
13. Las sales minerales no aportan energía, pero realizan importantes funciones a nivel celular y de organismo.
- Forma parte de los huesos, los dientes y los cartílagos (calcio, fósforo, magnesio y flúor).
- Regulan el equilibrio hídrico y electrolítico dentro y fuera de la célula, mediante la ósmosis.
- Intervienen en la excitabilidad nerviosa y en la actividad muscular (calcio y magnesio).
- Mediadores en la entrada de sustancias a la célula, como el Na que participa en la entrada de glucosa a la célula, necesaria en los procesos degradativos en los que se obtiene energía metabólica.
- El cromo posibilita la acción de la insulina.
- El selenio tiene acción antioxidante e interviene en el adecuado funcionamiento del sistema inmunológico, conjuntamente con el Zinc y el cobre.
- Forman parte de moléculas de gran importancia en el funcionamiento del organismo como un todo, por ejemplo: el hierro (Fe) forma parte de la hemoglobina de los glóbulos rojos de la sangre y el magnesio (Mg) de las moléculas de clorofila.
-Falso, no aportan energía a las células pero si cumplen otras funciones
14. Las moléculas que desvían la luz para la derecha son llamadas dextrógiras (D) y cuando el desvío es para la izquierda las moléculas son llamadas levogiras (L); la importancia de esto reside en el hecho de que una molécula dextrógira (D) y una levógira (L) de la misma substancia (DL) son imágenes de espejo una a la otra y como en bioquímica la disposición de los átomos es crucial en la determinación de la actividad biológica la misma substancia con distinta quiralidad (comportamiento diferenciado de dos entes que son simétricos) puede no presentar efectos biológicos similares, por ejemplo los aminoácidos biológicamente activos son siemprelevógiros (L) ya que los dextrógiros (D) no tienen acción biológica.

-E, una D y la otra L
15. Los péptidos son un tipo de moléculas formadas por la unión de varios aminoácidos mediante enlaces peptidicos.
Los péptidos, al igual que las proteínas están presentes en la naturaleza y son responsables por un gran número de funciones, muchas de las cuales todavía no se conocen.
La unión de un bajo número de aminoácidos da lugar a un péptido, y si el número es alto, a una proteína, aunque los límites entre ambos no están definidos. Orientativamente:
- Oligopéptido: De 2 a 10 aminoácidos.
- Polipetido: Entre 10 y 100 aminoácidos.
- Proteína: Más de 100 aminoácidos. Las proteínas con una sola cadena polipeptídica se denominan proteínas monoméricas, mientras que las compuestas de más de una cadena polipeptídica se conocen como proteínas multiméricas.
Ala-Met-Cys-Asn-Asn-Glu-Pro
Tyr-Gln-Asp-Asp-His- Gly-Tyr
-B, tienen distinta estructura primaria por su secuencia aminoácidos.
16. Proteína desnaturalizada: Se le llama a la desnaturalización de las proteínas a la perdida de estructuras de orden superior (secundaria, terciaria y cuartaría quedando la cadena perpendicular reducida a un polímero sin ninguna estructura tridimensional fija.
-A, se compone los enlaces y se pierden todas las estructuras salvo la primera.
17. El ARN es el que copia el material genético situado en el citoplasma, pero, se sintetiza en el núcleo.
-Falso, ya que se sintetiza en el núcleo, pero los ribosomas son quienes forman la cadena.
18. La molécula de la imagen es un esteroide, estos se componen de carbono e hidrógeno se sintetizan a partí del colesterol, tienen su lugar de acción en el ADN , activando genes o modulando la transcripción del ADN.
-B, es un esteroide, colesterol
19. La molécula de la imagen es un ALFA-AMINOÁCIDO NEUTRO POLAR, esto quiere decir que el grupo amino se encuentra ubicado en el carbono numero 2, neutro polar: hidrofilicas
-D, es un alfa-aminoácido neutro polar
20. Las sustancias hidrosolubles son las que contienen grupos lipófilos ya que los lipófilos tienen afinidad por los lípidos (grasas), por lo cual no son solubles en agua.
-Falso, ya que es graso y se convierte en no soluble.
21. El colágeno es una proteína con función estructural ya que la molécula proteica que esta compuesta por fibras o fibras colágenas. Se encuentran en todos los animales, son secretadas por células del tejido conjuntivo como los fibroplastos.
-Verdadero, ya que es la función estructural.
22. En la inhibición competitiva y no competitiva son mecanismos de regulación irreversibles de la actividad enzimáticas, en las que una molécula se une a un enzima y no inactiva parcialmente, consiste en que estos se unan al centro activo enzimático.
-Verdadero, en la inhibridacion competitiva el inhidrador se parece al sustrato.
23. Los disacáridos: Son un grupo de glúcidos formados por la unión de monosacáridos mediante un enlace O- glucosidico, si este enlace es monocarbonilo, será reductor, popr el contrario si es O-glicosidico, no será reductor.
-B,pierden el poder reductor al formarse enlaces O-glicosídico.
24.Las sales biliares son las sales de los ácidos biliares, pueden ser sales sódicas o potásicas Las sales biliares son la forma en que el cuerpo guarda los ácidos biliares en la vesícula biliar y son secretados al intestino para la digestión de lipidos.
-Verdadero,las sales biliares derivan del colesterol.
25. El Ácido ribonucleico está constituido por la unión de nucleótidos formados por una pentosa, la Ribosa, un bases nitrogenadas, que son Adenina, Guanina, Citosina y Uracilo. No aparece la Timina.
Los nucleótidos se unen formando una cadena con una ordenación en la que el primer nucleótido tiene libre el carbono 5’ de la pentosa. El último nucleótido tiene libre el carbono 3’. Por ello, se dice que la ordenación de la secuencia de nucleótidos va desde 5’ a 3’ (5’ ® 3’).
-A,ribonucleotidos 5` monofosfato de A,G,C y U
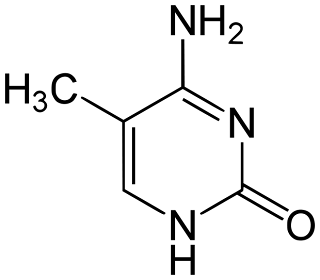
26.La molécula de la derecha es la citosina. La citosina se empareja con la guanina por medio de tres enlaces de hidrógeno.
-E,se une a la Guanina para formar un nucleótido.
27.Los polisacáridos: Son biomoleculas formadas por la unión de una gran cantidad de monosacaridos que se encuentran entre los glucidos y cumplen funciones diversas sobre todo de reservas energéticas y estructurales. Llevando a que los polisacáridos conserven las mismas propiedades físicas que los monosacaridos.
-A. conservan las mismas propiedades físicas que los monosacáridos.
28.Las sales minerales insolubles en agua, se encuentran principalmente en las estructuras oseas de los animales, también se pueden ser encontradas asociadas a otras moléculas.
-B,forman normalmente estructuras esqueléticas
29.Un lípido saponificable sería todo aquel que esté compuesto por un alcohol unido a uno o varios ácidos grasos (iguales o distintos). Esta unión se realiza mediante un enlace ester, muy difícil dehidrolizar. Pero puede romperse fácilmente si el lipido se encuentra en un medio básico. En este caso se produce la saponificación alcalina. En los casos en los que para la obtención del jabón se utiliza un glicerido o grasa neutra, se obtiene como subproducto el alcohol llamado glicerina, que puede dar mayor beneficio económico que el producto principal.
-Verdadero,la esterificación de la glicerina con ácidos grasos se llama saponificación.
30. Molécula anfipática: hace referencia a una estructura molecular que contiene dos propiedades, una hidrofílica (afinidad por el agua) y otra hidrofóbica (rechazo del agua). Estas moléculas son los principales constituyentes de la membrana celular, generando un sistema al que se le denomina mosaico fluido.
-Verdadero, las moléculas anfipaticas tienen una parte hidrofilica y otra hidrofobica